STABILITA SUSPENZIÍ A DISPERZIÍ – PREČO SÚ PARAMETRE AKO VEĽKOSŤ ČASTÍC, ZETA POTENCIÁL A REOLOGICKÉ VLASTNOSTI TAKÉ DÔLEŽITÉ?
V prípade suspenzií s veľkosťou častíc menšou ako 1 mikrometer je Brownov pohyb zvyčajne nevyhnutný na udržanie častíc v disperznej fáze, avšak v prípade väčších častíc sa účinok gravitácie stáva dôležitým, ak existuje významný rozdiel v hustote disperznej a kontinuálnej fázy. V takom prípade možno pravdepodobnosť sedimentácie predpovedať z pomeru gravitačnej a Brownovej sily pomocou rovnice 1 [1].
![]()
Reológia – stabilita suspenzie
Kde a je polomer častice, Δρ je rozdiel hustoty medzi disperznou a spojitou fázou, g je gravitačné zrýchlenie, kB je Boltzmannova konštanta a T je teplota.
Ak je tento pomer väčší ako jedna, možno očakávať určitý stupeň sedimentácie, zatiaľ čo pomer menší ako jedna bude pravdepodobne znamenať stabilný systém. Táto rovnica však nezohľadňuje potenciálne interakcie medzi časticami. V dôsledku Brownovho pohybu budú častice neustále do seba narážať a v dôsledku toho sa môžu častice zhlukovať v dôsledku Van der Waalsových príťažlivých síl. To môže viesť k vzniku sekundárnych častíc (vločiek) s oveľa väčšou veľkosťou, a teda s väčším príspevkom gravitácie do rovnice 1, s následným usadzovaním.

Obr. 1 – Bloková schéma znázorňujúca zmeny voľnej energie pri separácii častíc pre suspenziu s (a) vysokým zeta potenciálom (b) nízkym zeta potenciálom
Aby sa zabránilo zhlukovaniu častíc, je potrebné zabezpečiť určitú bariéru. To možno dosiahnuť priestorovými alebo elektrostatickými prostriedkami adsorpciou polymérov alebo zavedením náboja na povrch častíc, napríklad úpravou pH. Ak odpudivá sila prevyšuje príťažlivú silu, mal by vzniknúť stabilný systém. Pre elektricky nabitú suspenziu možno takýto princíp rovnováhy síl opísať teóriou DLVO, kde kombinovaná/celková energia (VT) je súčtom príspevkov príťažlivej (VA) a odpudivej sily (VR), ako je znázornené na obr. 1a. Táto teória navrhuje, že energetická bariéra vyplývajúca z odpudivej sily zabráni dvom časticiam priblížiť sa k sebe a zlepiť sa, pokiaľ častice nemajú dostatočnú tepelnú energiu na prekonanie tejto bariéry.
Veľkosť tejto potenciálnej bariéry možno vyjadriť veľkosťou zeta potenciálu, čo je potenciál v rovine sklzu medzi časticou a pridruženou dvojvrstvou s okolitým rozpúšťadlom [4, 5]. Ak majú všetky častice v suspenzii vysoký záporný alebo kladný zeta potenciál, budú mať tendenciu sa navzájom odpudzovať a častice nebudú mať tendenciu agregovať. Ak však majú častice nízke hodnoty zeta potenciálu, potom odpudzovanie nebude dostatočné na to, aby zabránilo zhlukovaniu častíc a ich zrážaniu vo forme vločiek. Všeobecná deliaca čiara medzi stabilnou a nestabilnou suspenziou sa zvyčajne považuje za +30 alebo -30 mV a častice, ktoré majú zeta potenciál mimo týchto hraníc, sa zvyčajne považujú za stabilné [6, 7]. Takýto predpoklad však veľmi závisí od vlastností častíc [1, 4]. V tomto článku uvažujeme o význame veľkosti častíc, zeta potenciálu a reológie na sedimentačné správanie a ukazujeme, ako možno tieto vlastnosti manipulovať na vyvolanie stability.
Experimentálna časť
V tejto štúdii sa použila vzorka mikrokryštalického oxidu kremičitého s hustotou 2,6 g/cm3 a Dv(50) 3,7 μm, ako sa meralo na prístroji Malvern Mastersizer 2000 s disperznou jednotkou Hydro S. Tieto vzorky sa hodnotili pomocou meraní zeta potenciálu austálenej smykovej reológie na posúdenie stability v závislosti od pH. Na meranie zeta potenciálu pomocou prístroja Malvern Zetasizer Nano ZS v spojení s autotitrátorom MPT2 sa na analýzu pripravila zriedená disperzia materiálu v deionizovanej vode. Titrátor sa naplnil 0,25 M a 0,025 M HCl na titráciu od počiatočného pH vzorky po konečné pH 1,0 a zaznamenali sa 3 opakované merania zeta potenciálu v 10 rovnakých intervaloch pH v celom rozsahu. Všetky testy sa vykonali pri teplote 25 °C. Reologické merania sa vykonali s koncentrovanými disperziami (75 % hmotnosti) vzorky oxidu kremičitého v deionizovanej vode. pH vzoriek sa upravilo pomocou HCl tak, aby sa dosiahli hodnoty ekvivalentné hodnotám použitým pri štúdii zeta potenciálu. Reologické testy sa vykonali na reometri Kinexus Pro a Gemini 2 s použitím paralelných drážkovaných platní a pracovnej štrbiny 0,5 mm. So vzorkami sa vykonali dva typy testov vrátane testu rovnovážnej skokovej šmykovej rýchlosti a testu rampy šmykového napätia. Prvý test zahŕňal skokové zvýšenie šmykovej rýchlosti v rozsahu od 0,1 do 100 s-1 s cieľom vytvoriť krivku toku (viskozita v závislosti od šmykovej rýchlosti). Druhý test zahŕňal použitie lineárne rastúcej rampy smykového napätia od 0 do 100 Pa počas 60 s na určenie hranice toku (medze klzu). Všetky testy sa vykonali pri teplote 25 °C.
Výsledky a diskusia
Na obrázku 2 je znázornený vplyv pH na suspenziu častíc oxidu kremičitého rozptýlených v deionizovanej vode s priemernou veľkosťou častíc 3,7 μm, ako sa stanovilo pomocou prístroja Mastersizer 2000.
Napriek tomu, že táto suspenzia mala záporný zeta potenciál viac ako 30 mV, ukázalo sa, že je nestabilná a pri státí vytvára kompaktnú vrstvu sedimentu. Ak sa príslušné parametre častíc/tekutiny dosadia do rovnice 1, pomer gravitácie a Brownovej sily vychádza viac ako 45. To naznačuje, že gravitačné sily sú vysoko dominantné, a preto sa neočakáva, že zeta potenciál významne ovplyvní stabilitu sedimentu. Z tej istej rovnice vyplýva, že Brownove sily sú dominantné len pre častice s priemerom menším ako približne 1,5 μm. Keď v systéme dominujú gravitačné sily riadené veľkosťou a hustotou častíc, elektrostatické interakcie už nebudú stačiť na zabezpečenie stability, a preto sú potrebné iné spôsoby stabilizácie.
Jedným zo spôsobov je zvýšenie kinetickej stability suspenzie spomalením rýchlosti sedimentácie. To možno dosiahnuť zvýšením viskozity kontinuálnej fázy. Rýchlosť sedimentácie sa potom môže predbežne vypočítať pomocou Stokesovho zákona (rovnica 2) za predpokladu zriedenej suspenzie sférických častíc [2].

Stokesov zákon
Kde V predstavuje rýchlosť sedimentácie a η predstavuje šmykovú viskozitu kontinuálnej fázy. Preto zdvojnásobenie viskozity zníži rýchlosť sedimentácie o rovnaký faktor, zatiaľ čo polovičná veľkosť častíc zníži rýchlosť sedimentácie o faktor 4. Tieto výrazy sú však použiteľné len pre zriedené suspenzie, kde sú interakcie častíc minimálne. Sedimentácia koncentrovaných suspenzií je komplikovanejšia v dôsledku interakcií medzi susednými časticami a skutočnosti, že vysoký obsah častíc vedie k zvýšeniu celkovej hustoty a viskozity.
Existuje niekoľko rovníc na predpovedanie rýchlosti sedimentácie v koncentrovaných disperziách, pričom jedna z nich (rovnica 3) je modifikáciou Stokesovej rovnice, kde φ predstavuje objemový podiel a exponent sa mení s veľkosťou častíc, pričom hodnoty sú približne 5,25 pre častice väčšie ako 1 μm a 4,75 pre častice menšie ako 1 μm [2].
![]()
Modifikácia Stokesovej rovnice
Náboj na častici môže tiež zohrávať významnú úlohu pri spomaľovaní sedimentácie, pretože súvisiaca elektrostatická vrstva bude mať konečnú hrúbku, ktorá zvýši efektívny fázový objem dispergovanej fázy. Tento účinok bude výraznejší v prípade menších častíc [1, 2].
Ďalším spôsobom, ako navodiť stabilitu v suspenziách, v ktorých dominujú gravitačné sily, je zaviesť do systému sieťovú štruktúru, a teda limit toku. Jedným zo spôsobov, ako to dosiahnuť, je želatínovanie kontinuálnej fázy pomocou vhodných prísad. Iným prístupom, ktorý sa môže zdať kontraproduktívny, je zníženie odpudzovania medzi časticami, a tým vlastne podpora flokulačnej sily v systéme, ako je znázornené na obr. 1b. O tomto druhom prístupe sa bude hovoriť podrobnejšie. Z obr. 2 je zrejmé, že zníženie pH znižuje zeta potenciál, pričom izoelektrický bod je pri pH 1,17. Vplyv takejto zmeny na reológiu je možné demonštrovať na obr. 3, na ktorom je znázornená šmyková viskozita ako funkcia šmykovej rýchlosti pre rôzne vzorky. Pri pH 3,9 je viskozita relatívne nízka a so zvyšujúcou sa rýchlosťou strihu dochádza k miernemu poklesu viskozity, čo svedčí o nenewtonovskom alebo strihovom riedení. Mierne vyššia úroveň ustálenej viskozity pri nižších smykových rýchlostiach sa nazýva nulová smyková viskozita a je spôsobená náhodnou orientáciou častíc pri nízkych smykových rýchlostiach a nárastom efektívneho fázového objemu v dôsledku náboja častíc. Pri vyšších smykových rýchlostiach sa hydrodynamické faktory stávajú dominantnými s následnou zmenou usporiadania disperznej fázy a následným poklesom viskozity [1].
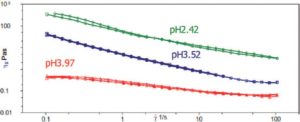
Obr. 3 Viskozita v závislosti od smykovej rýchlosti pre rôzne vzorky
S ďalším poklesom pH sa viskozita zvyšuje a táto stabilná úroveň nízkej šmykovej viskozity už nie je viditeľná. To naznačuje, že materiál vykazuje pevné správanie odvodené od neprítomnosti tejto stabilnej nízkej úrovne šmykovej viskozity; hoci na potvrdenie tohto tvrdenia by bolo potrebné vykonať meranie pri nižšej šmykovej rýchlosti.
Opakovanie tej istej skúšky s predtým strihanými vzorkami dáva vo všetkých prípadoch takmer identické krivky toku, čo naznačuje, že tieto vzorky nie sú trvalo strihané, ale vytvárajú dočasnú sieťovú štruktúru, ktorá rýchlo koriguje následné narušenie. Toto sa potvrdilo z trojstupňového testu smykovej rýchlosti, ktorým sa určuje viskozita pri nízkej smykovej rýchlosti a potom sa meria čas potrebný na obnovenie tejto viskozity po určitom čase namáhania smykom pri vysokej smykovej rýchlosti. Takýto test je znázornený na obrázku 4 pre vzorku s pH 4 s použitím počiatočnej/konečnej smykovej rýchlosti 0,1 s-1 a strednej smykovej rýchlosti 10 s-1. Z toho vyplýva, že vzorka takmer okamžite obnoví svoju viskozitu, hoci má o niečo vyššiu viskozitu, ako sa pôvodne pozorovalo, čo je pravdepodobne spôsobené reorganizáciou mikroštruktúry.
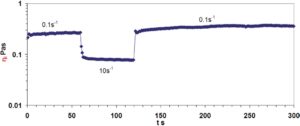
Výsledky testu šmykovej rýchlosti pre vzorku pripravenú pri pH 4
Túto reverzibilnú flokuláciu možno vysvetliť teóriou DLVO. Znížením povrchového náboja častíc sa znižuje príspevok odpudzovania k celkovému interakčnému potenciálu. To vedie k vytvoreniu sekundárneho minima na krivke potenciálnej energie, ako je znázornené na obrázku 1b, ktoré pripúšťa oveľa slabšiu a reverzibilnú adhéziu medzi časticami. Tieto interakcie sú dostatočne silné na to, aby odolali účinkom Brownovho pohybu, ale zároveň dostatočne slabé na to, aby sa rozpadli, keď sa aplikuje strih. Hĺbka tohto sekundárneho minima zohráva rozhodujúcu úlohu pri určovaní štruktúry vločiek a následne potenciálu pre tvorbu siete. Keď je toto sekundárne minimum relatívne hlboké, t. j. 10 až 20 kT, zrážajúce sa častice sa na seba silno naviažu a vytvoria otvorenú štruktúru s väčším fázovým objemom, čo je priaznivé pre tvorbu siete. Naopak, slabo vločkovité systémy sú schopné sa lokálne preskupovať a vytvárať hustejšie vločky, ktoré skôr sedimentujú [1, 2].
Sila tejto sieťovej štruktúry sa môže prejaviť v medziplyne, čo je sila potrebná na prekonanie týchto príťažlivých síl a iniciovanie tečenia.
Pomocou reometra existuje niekoľko experimentálnych testov na určenie hranice toku. Jednou z najrýchlejších a najjednoduchších metód je vykonanie šmykového napätia a určenie sily, pri ktorej sa pozoruje maximálna viskozita. Pozorovaný nárast viskozity pred týmto maximom je výsledkom pružnej deformácie (deformačného spevnenia); maximálna hodnota preto predstavuje bod, v ktorom táto pružná štruktúra ustupuje.
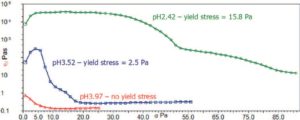
Obr. 5 Meranie hranice toku pre vzorky pripravené pri rôznych hodnotách pH
Na obrázku 5 je vidieť, že dve vzorky s nízkym pH vykazujú maximálnu viskozitu, čo svedčí o hranici toku. Aj sila, pri ktorej sa toto maximum vyskytuje, je oveľa vyššia pre vzorku s nízkym pH, čo naznačuje, že pevnosť štruktúry sa zvyšuje s klesajúcim zeta potenciálom. Pri vzorke s vysokým pH sa nevyskytuje žiadne viskozitné maximum, čo naznačuje, že tento materiál nemá žiadne obmedzenie toku, a teda ani sieťovú štruktúru. V druhom prípade možno rýchlosť sedimentácie odhadnúť z rovnice 3, zatiaľ čo v prípade časticového gélu je termodynamická stabilita výsledkom len vtedy, keď sila pôsobiaca na štruktúru je pod touto hranicou toku. Odhad sily pôsobiacej časticou na jej okolie možno získať z rovnice 4, kde ρD je hustota disperznej fázy a ρC je hustota spojitej fázy.

Odhad sily, ktorou častica pôsobí na svoje okolie
Pre suspenziu oxidu kremičitého použitú v tejto štúdii je vypočítaná hodnota približne 0,01 Pa pre najväčšiu časticu, ktorá má priemer približne 10 μm. V dôsledku toho by tieto systémy s nízkym pH mali byť stabilné voči sedimentácii za ustálených podmienok, hoci je potrebné vziať do úvahy aj sily vyplývajúce z vonkajších porúch, ako sú tie, ktoré sa vyskytujú počas prepravy.
Zdróje
[1] Larson, R.G (1999), The Structure and Rheology of Complex Fluids, Oxford University Press, New York.
[2] Barnes, H.A (2000), A Handbook of Elementary Rheology, University of Wales, Institute of Non-Newtonian Fluid Mechanics.
[3] Hunter, R.J (1988), Zeta Potential in Colloid Science: Principles and Applications, Academic Press, UK.
[4] B. Derjaguin, L. Landau (1941) Theory of the stability of strongly charged lyophobic salts and of the adhesion of strongly charged particles in solutions of electrolytes, Acta Physico Chemica URSS 14, 633.
[5] E.J.W. Verwey a J. Th. G. Overbeek (1948) Theory of the stability of lyophobic colloids, Elsevier, Amsterdam.
[6] Zeta potenciál za 30 minút, technická poznámka dostupná na www.malvern.com.
[7] Zeta potenciál koloidov vo vode a odpadových vodách, norma ASTM D 4187-82, Americká spoločnosť pre testovanie a materiály, 1985

